Lombalgies et dorsalgies d’origine musculaire
IntķrĻt de
l'ķcho-tomographie
J.G.
Drevet* G. Kern* X. Phelip*
Les douleurs
rachidiennes, de nature mķcanique, traduisent des phķnomĶnes pathologiques
variķs, intķressant de fańon isolķe ou associķe les structures discales,
articulaires postķrieures, mais ķgalement pķri-articulaires : les tendons,
les ligaments et les muscles. La responsabilitķ des chaŅnes musculaires
postķrieures apparaŅt sous estimķe et frķquemment mķconnue.
L'ķchotomographie musculaire, qui a fait la preuve de son intķrĻt dans la
pathologie musculaire et tendineuse pķriphķrique, est susceptible
d'objectiver des lķsions des chaŅnes musculaires Ó l'origine de tableaux
douloureux persistants.
1)
Caractķristiques cliniques
Plusieurs
ķlķments cliniques permettent de suspecter la responsabilitķ des chaŅnes
musculaires, face Ó un tableau douloureux dorsal ou lombaire
a) L'existence
d'une zone ½ gŌchette ╗ musculaire para-vertķbrale
Conduite de
fańon minutieuse, la palpation des chaŅnes musculaires dorsales et lombaires
postķrieures dķcĶle une zone souvent ponctuelle, trĶs circonscrite, dont la
pression maintenue rķveille ou exacerbe les douleurs habituellement
ressenties. Les douleurs spontanķes peuvent Ļtre diffuses et bilatķrales ou
latķralisķes du c¶tķ porteur de la zone gŌchette. Soulignons que l'existence
de ce secteur musculaire, exacerbant les douleurs, est en rĶgle mķconnue du
patient, ce qui souligne l'intķrĻt de sa recherche systķmatique.
b) L'anesthķsie
de ce territoire musculaire contr¶le tout ou partie des douleurs
Une faible
quantitķ de lidocaine, de l'ordre de 1 ml, permet de neutraliser le
territoire musculaire douloureux identifiķ et de constater une diminution
importante des douleurs habituellement ressenties.
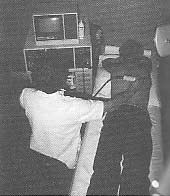
Fig. 1 : conduite de l'ķchotomographie, le patient ķtant en procubitus.
c) A l'opposķ,
l'injection d'une substance placebo
au niveau de ce territoire musculaire isolķ n'est suivie d'aucun effet
favorable. Ce test, qui peut Ļtre effectuķ Ó distance ou prķcķder
l'injection par le produit anesthķsique, permet une meilleure sķlection des
indications de l'ķchotomographie.
d) Les
dorso-lombalgies apparaissent isolķes
La recherche
d'une souffrance vertķbrale, de nature discale ou articulaire postķrieure,
se rķvĶle nķgative. De mĻme une autre ķtiologie mķcanique, notamment
ligamentaire, aura ķtķ ķliminķe, ainsi que les affections inflammatoires,
les pathologies viscķrales Ó expression rachidienne...
2)
L'ķtude ķchotomographique
a) La conduite
pratique de l'examen
nķcessite une
ķtude comparative des chaŅnes musculaires, par la rķalisation de coupes
axiales et transversales (fig. 1). Des ķpreuves statiques et dynamiques de
contractions volontaires des muscles para-vertķbraux permettent, d'une part,
de sensibiliser l'examen, d'autre part, de dķpister d'ķventuelles
contractures musculaires organisķes.
b)
L'appareillage utilisķ
est habituellement un ķchoŁtomographe en temps rķel, muni d'une sonde d'une
frķquence de 6 Ó 7.5 mķgahertz. Le dķpistage et l'analyse des anomalies
ķchotomographiques peuvent prķsenter des difficultķs et nķcessitent d'Ļtre
effectuķs par un radiologue expķrimentķ.
Plusieurs
anomalies ķchotomographiques peuvent alors Ļtre objectivķes rķalisant des
territoires hyperŁķchogĶnes ou hypo ķchogĶnes.
3)
Rķsultats
a) les
territoires hyper ķchogĶnes
Ces plages hyper
ķchogĶnes sont distantes de 50 Ó 110 mm de l'axe des ķpineuses, en regard du
rachis dorsal ou du rachis lombaire. Les contours sont irrķguliers, parfois
uniques (fig.2), ou multiples (fig.3) ; les dimensions sont en rĶgle
modestes, ne dķpassant pas 30 mm de long et 10 mm de largeur, dans notre
expķrience (fig. 4 et 5).
Ces anomalies
concernent les groupes musculaiŁres superficiels : les plages hyper
ķchogĶnes sont, en effet, distantes de 20 Ó 35 mm du revĻtement cutanķ. Il
est possible de constater des foyers hyper ķchogĶnes au sein des muscles
fessiers, rķpondant Ó des critĶres identiques de sķlection (Fig. 6, 7 et
8).L'image ķchotomographique ainsi individualiŁsķe peut Ļtre assimilķe au
territoire musculaire qu'isole l'examen clinique ; en effet, un contr¶le
peut Ļtre rķalisķ en effectuant une infiltration anesŁthķsique lors de la
rķalisation de l'ķchotomographie, permettant de guider la position de
l'aiguille.
Fig. 2 : territoire hyper ķchogĶne responsable de dorsalgies chroniques,
installķes depuis plusieurs annķes, au dķcours d'un traumatisme ayant
concernķ les chaŅnes musculaires dorsales.
Fig. 3 Plusieurs plages hyperķchogĶnes, de petites dimensions, rendent
compte de douleurs dorso‑lombaires, unilatķrales : leur anesthķsie
sķlecŁtive est suivie d'une disparition des dolķances.
Fig 4 Coupes transversales, permettant l'analyse comparative des masses
musculaires, situķes de part et d'attire de la projection de l'axe des
ķpineuses : foyers hyperķchogĶnes droits
Fig. 5 : image centrķe
sur le secteur pathologique.
Fig. 6 et 7 Plage hyperķchogĶne isolķe, siķgeant dans le muscle fessier
(Fig. 6), responsable de lombalgies basses unilatķrales, contrastant avec
l'intķgritķ du muscle controlatķral (Fig. 7).
Les patients
porteurs de territoires hyper ķchogĶnes prķsentent parfois des antķcķdents
traumatiques francs, susceptibles d'avoir concernķ les chaŅnes musculaires
douloureuses. Cela n'est cependant pas constant, bien que constituant une
orientation diagnostique. En effet, ces territoires hyper ķchogĶnes peuvent,
certes, traduire un processus iatrogĶne d¹ Ó l'injection de produits
sclķrosants.
En dehors de
cette hypothĶse, la plage hyper ķchogĶne ķvoque alors un granulome
cicatriciel, s'exprimant par un processus fibreux ; cette ķtiologie prend
toute sa valeur dans nos observations pour lesquelles aucune injection de
produits sclķrosants n'a ķtķ effectuķe. Les images observķes sont par
ailleurs trĶs proches de celles constatķes dans la pathologie pķriphķrique
post-traumatique.
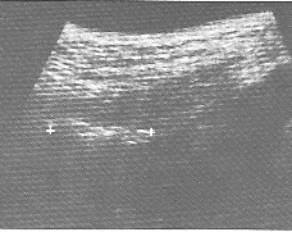 Fig.
8 Lombalgies rebelles aux traitements mķdicaux, secondaires Ó un traumatisme
de la rķgion lombo-fessiĶre, liķes Ó une plage hyperķchogĶne, ķvocatrice
d'un granulome cicatriciel.
Fig.
8 Lombalgies rebelles aux traitements mķdicaux, secondaires Ó un traumatisme
de la rķgion lombo-fessiĶre, liķes Ó une plage hyperķchogĶne, ķvocatrice
d'un granulome cicatriciel.
b) Les
territoires hypoķchogĶnes
Des critĶres
cliniques identiques Ó ceux utilisķs pour la localisation des plages
musculaires hyperķchogĶnes peuvent permettre l'individualisation de
territoires hypoķchogĶnes : zone "gŌchette" musculaire para-vertķbrale dont
l'anesthķsie attķnue les douleurs habituellement ressenties, une substance
placebo se rķvķlant inefficace.
Il
n'existe, ainsi, pas d'ķlķment clinique susceptible d'orienter plus vers la
dķcouverte de plages hypo-ķchogĶnes ou hyperŁķchogĶnes, en dehors de la
possibilitķ, dans les antķcķdents, d'un traumatisme direct des chaŅnes
musculaires para-vertķbrales, ķvocateur d'un granulome cicatriciel.
Ces anomalies
ķchographiques concernent ķgalement les muscles superficiels, assez proches
de l'axe rachidien. La distance par rapport au revĻtement cutanķ varie de 15
Ó 35 mm et, par rapport Ó l'axe des ķpineuses, de 20 Ó 110 mm. Les plages
hypoķchogĶnes sont habituellement de forme ovo’de (fig.9), parfois sphķrique
(fig.10) ; les contours sont irrķguliers, les limites imprķcises (fig.11).
Leurs dimensions sont relativement peu importantes : 15 Ó 35 mm d'ķpaisseur
et 20 Ó 40 mm de longueur. Aucune plage anķchogĶne n'a ķtķ constatķe.
Fig. 9 Secteur hypoķchogĶne de siĶge lombaire, correspondant Ó la zone
½ gŌchette ╗ isolķe par l'examen
clinique des chaŅnes musculaires.
Fig. 10 Plage hypoķchogĶne ovo’de et
superficielle.
Fig. 11 Territoire hypoķchogĶne de forme sphķrique, aux limites imprķcises
Les douleurs
sont d'installation progressive, les patients ne pouvant reconnaŅtre
un facteur dķclenchant prķcis ; le dķbut des manifestations cliniques est
ainsi rarement brutal, ķvocateur d'une pathologie d'effort, comme le suggĶre
l'observation suivante :
Un jeune skieur
de compķtition souffre de lombalgies latķralisķes Ó gauche depuis 3 mois,
d'intensitķ croissante, apparues lors d'un entraŅnement sportif. L'examen
clinique, ainsi que les radiographies du rachis dorso-lombaire, ne
permettent pas de retenir une ķtiologie particuliĶre; cependant, l'analyse
des chaŅnes musculaires, en regard du rachis lombaire bas, dķcĶle 1 secteur,
situķ Ó quelques centimĶtres de la ligne des ķpineuses, dont la pression
exacerbe les douleurs habituelles. L'ķchotomographie dķcĶle, en regard de ce
secteur, une plage hypo ķchogĶne (Fig. 12) dont l'anesthķsie soulage
temporairement le patient.
L'absence
d'anomalie ķchographique
peut Ļtre
constatķe, malgrķ le respect des critĶres de sķlection clinique ; en effet,
chez prĶs de 20 % des sujets examinķs (4), l'examen ķchographique se rķvĶle
strictement normal, ce qui incite Ó envisager une limite technique de
l'examen : des lķsions trĶs limitķes ou dķbutantes peuvent ne pas avoir de
traduction ķchotomographique, de mĻme, les secteurs musculaires profonds
ķchappent Ó l'analyse.
Signification
des territoires hypo ķchogĶnes
L'interprķtation
de l'hypoķchogķnķcitķ apparaŅt dķlicate : une contracture musculaire
prķsente une disŁposition plus fasciculaire que focale ; une solution de
continuitķ des fibres musculaires, une collection liquidienne (pour les
images aux contours les plus prķcis), une adipose Ó faible composante
conjonctive peuvent Ļtre ķvoquķes.
C'est pourquoi,
nous avons effectuķ, chez cinq sujets volontaires, une ķtude
histo-morphomķtrique des sites musculaires individualisķs par
l'ķchotomographie, selon un protocole standard : rķactions
histoŁenzymatiques sur matķriel congelķ, dķtection en immuno-fluorescence
d'ķventuels dķp¶ts d'immunoŁglobulines, analyse morphomķtrique, examen en
microscopie photonique et ķlectronique du matķriel inclus dans l'ķpon.
- Des dķp¶ts
adipeux sont rencontrķs en situation pķrimysiale, endomysiale ou sous forme
de globuŁles lipidiques intra‑sarcolķmiques.
- L'atteinte de
type myogĶne est constante : hypoŁtrophie des fibres musculaires, vacuoles
autophaŁgiques isolķes, dķsorganisation de la bande Z, anomalies
mitochondriales... Il s'y associe, dans 4 cas, des lķsions de type neurogĶne
pķriphķrique, suggķrant une soufŁfrance des branches nerveuses postķrieures.
Fassbender et Wegner6 constataient, en 1973 des anomalies de type
myogĶne chez des patients souffrant de douleurs musculaires persistantes.
Nos rķsultats se rapprochent des leurs, quant a l'origine myogĶne des
lķsions. Les auteurs ķvoquent une hypoxie des cellules musculaires,
consŁtatant ultķrieurement des altķrations des capillaires endomysiaux5,
que nous n'avons pas observķes.
Les dķp¶ts
adipeux au sein des fibres musculaires ont ķtķ dķcrits par plusieurs auteurs3,11,
interprķtķs comme une dķgķnķrescence graisseuŁse. Awad2 fait
ķtat, en 1973, de la prķsence d'adipose dans quelques biopsies rķalisķes au
sein des muscles quadriceps et trapĶzes. L'intensitķ des dķp¶ts adipeux dans
les muscles hypoķchogĶnes est variable mais elle autorise l'ķtablissement
d'une relation entre l'hypodensitķ ķchotomographique et la prķsence
d'adipose endomysiale.
S'agit-il d'une
pathologie prķcķdemment individualisķe ?
Travell et
Simons14,16, sous le terme de myofiascial trigger point,
regroupent les notions anciennes de myofascitis1,7,15, myalgic
spot9, interstitial myofibrositis2, rheumatic myalgia8,
myogķlose13, fibrositis10, muskel-schwiele12.
Cette pathologie comporte plusieurs critĶres cliniques dont les principaux
sont :
• une tension
musculaire trĶs localisķe, palpable pouvant rķaliser des formations
nodulaires trĶs perceptibles ;
• l'existence de
douleurs rķfķrķes, parfois trĶs Ó distance ;
• des phķnomĶnes
vaso-moteurs, apparaissant plus accessoires ;
Ces critĶres ne
s'appliquent que partiellement aux patients porteurs de plages
hypoķchogĶnes, la palpation ne relevant pas, de fańon rķguliĶre,
d'induration localisķe.
Conclusion
L'ķchotomographie permet d'objectiver, chez certains sujets souffrant de
lombalgies ou de dorsalgies, des altķrations musculaires paravertķbrales, se
traduisant par des territoires hyper ou hypoķŁchogĶnes, constituant le site
essentiel des phķnomĶnes douloureux,
Les territoires
hyperķchogĶnes sont en faveur de granulomes cicatriciels, les plages
hypoķchogĶnes traduisant, chez certains sujets, une adipose pķrimysiale et
endomysiale, associķe Ó des signes d'atrophie de type myogĶne, Soulignons
que des anomalies trĶs proches des prķcķdentes peuvent ķgalement Ļtre
observķes Ó l'ķtage cervical. Il apparaŅt ainsi que la dķmarche clinique
peut intķgrer les signes ķvocateurs d'une souffrance des chaŅnes musculaires
pķri-rachidiennes, que confirmera, frķquemment, la rķalisation de l'examen
ķchotomographique.
Bibliographie
1
ADAMS R.D.
Diseases of muscle: a study in pathology. 3ķdit. New York, Harper and Row
(Hagerstown) 1985.
2
AWAD E.A.
Interstitial myofibrositis : hypothesis of the mechanism. Arch. Phys. Med.,
1973, 54, 440-453.
3
BRENDSTRUP P., JESPERSEN K., ASBOE-HANSEN G. Morphological and chemical
connective tissue changes in fibrositis muscles Ann Rh. Dis.
1957,16,438-440.
4
DREVET J.G., PHELIP X., KERN G., STOEBNER P., CHIROSSEL J.P.
Echotomographie
musculaire. Approche ķtiologique de certaines lombalgies. Rev. Rh Mal.
Ostķoartic., 1985,52,397-402.
5
FASSBENDER H.G.
Pathology of rheumatic diseases. New York, Springer Verlag, 1975.
6
FASSBENDER H.G., WEGNER K.
Morphologie und Pathogenese des Weichteilrheumatismus. Z. Rheum forschg.,
1973 32,355-374.
7
GILLETTE HZ
Office management of musculoskeletal pain. Texas State J. Med.,
1966,62,47-53.
8
GOODM.G.
Die
primõre Rolle des Muskulatur in der Pathogenese der theumatischen Krankheit
und die therapeutische L÷sung des Rhaumaproblems. Mediz³lische (Stuttgart),
1957,13,450-454.
9
GUTSTEIN M.
Diagnosis and Treatment of muscular rheumatism. Br. J. Phys. Med.,
1938,1,302-321.
10
KRAFT G.H., JOHNSON E.W., LABAN MM.
The
fibrositis syndrome. Arch. Phys. Med.
Rehab., 1968,49,155-162.
11
MIEHLKE K., SCHULZE G., EGE W.
Klinische und experimentelle Untersuchungen zum FibrositisŁsyndrom.. Z.
Rh.f..h., 1960,19,310-330.
12
MULLER A.
Der
Vntersuchungsbefund am rheumatisch erlaanten Muskel. Z. Min. Med.,
1912,74,34-73.
13
SCHADE H.. Untersuchungern in der ErkŌltungstrage 111. Ober den
Rheumatismus, insbesondere den Musker1rheumatismus (Myogelose). M³nch. Med.
Wscher., 1921,68,95-99.
14
SIMONS D.G..
Muscle
pain syndromes. Am. J. Phys. Med., 1975,54,289-311.
15
SOLA A.E., KUITERT J.H.
Quadratus lumborum myofascitis. Northwest Med., 1954,53,1003-1005.
16
TRAVELL H., SIMONS D.G.
Myo
fascial pain and dysfunction : the trigger point manual. Baltimore, Williams
and Wilkins, 1983.
